单来说说近期echosens推送的两篇文章,第一篇是FIB-4联合VCTE预测在糖尿病合并MASLD人群进展期纤维化及长期预后结局第二篇是首个能够识别纤维化MASH组织学缓解并预测LREs的无创模型发布。
温馨提示:福瑞医科并不在Ai医疗热点上,看到这篇文章真想买Ai医疗的人请去迪安诊断等股,这股并不适合做短线
这两篇文章,虽然本质还是借助Fibroscan干“诊断”工作,但其核心价值在于FibroScan的检测场景从传统的“肝病科确诊”前移并融入至更广泛的“代谢病(糖尿病)全病程管理”中,拓宽了FibroScan的适用边界与受众基数。代谢是一个很大的话题,希望关注福瑞的医生能出来给大家讲讲。常见代谢病例如肥胖,高血脂,甲减,心血管代谢综合征等,只要涉及到与肝脏有关代谢的疾病,就有给患者做Fibroscan并预测患者预后的价值,可以搞清楚代谢治疗(减肥/控糖/降脂)是否真的改善了患者全身健康。例如,肥胖症: 监测减重过程中,内脏脂肪(CAP值)与肝脏应力(LSM值)的改善情况,验证“健康瘦身”。高脂血症与甲减: 评估降脂药或甲状腺激素替代治疗是否成功逆转了肝脏的代谢压力。
第一篇文章通过FIB-4联合LSM的“两步法”策略,在糖尿病合并MASLD人群中能有效实现进展期纤维化风险分层和长期预后预测。第二篇文章通过FibroScan的检测结果与肾功能(肌酐)绑定,查肝的同时顺便评估了代谢对肾脏的潜在综合影响,进一步将FibroScan从“查肝病”推向了“查代谢综合征”,有利于Fibroscan在非肝病专科(如全科、内分泌科)推广
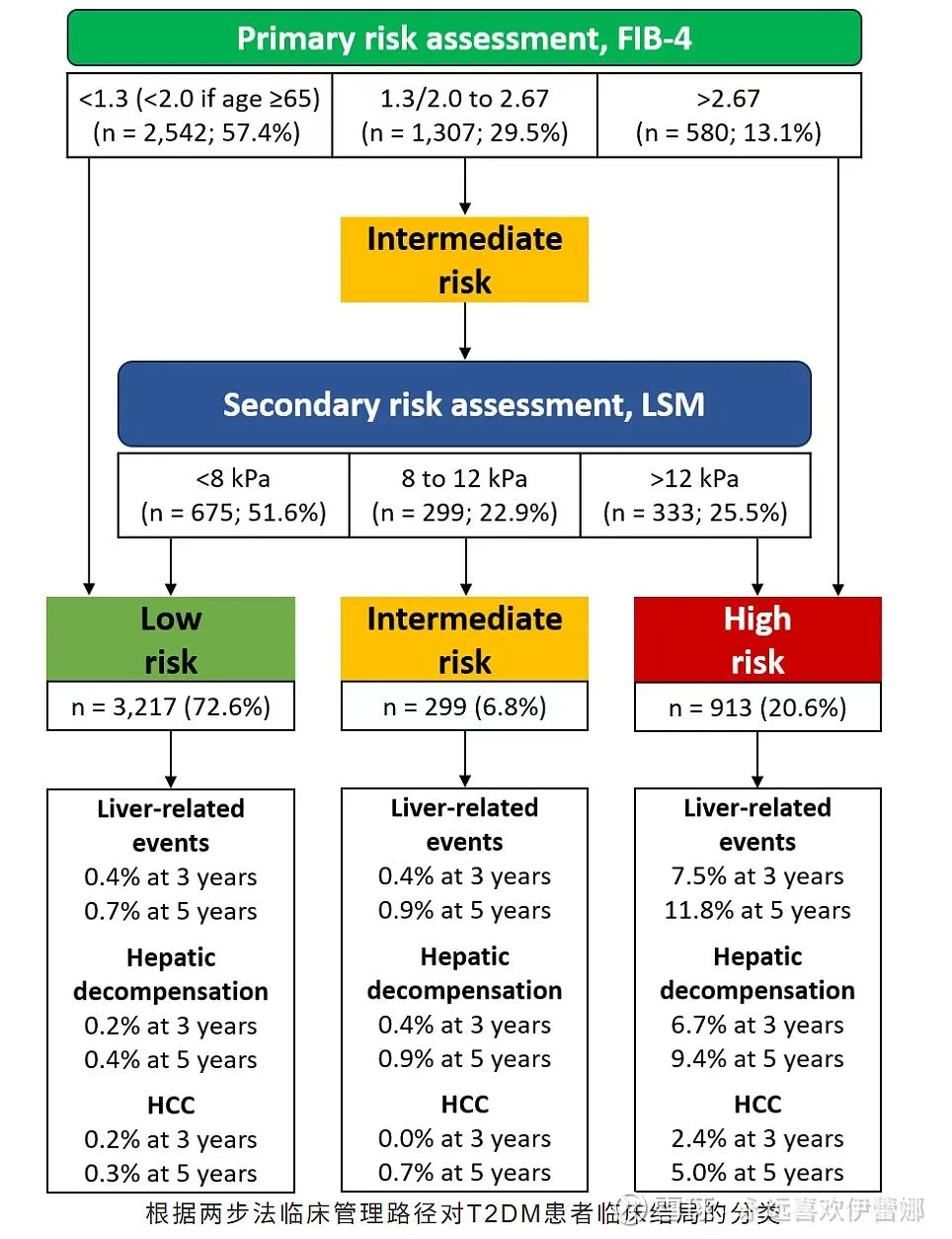
简单来说,这两篇文章是在扩大患者来源,但其检测与评估方法仍然是“静态的”
三、动态监测的范式冲突:循证医学遭遇数据科学。虽然Fibroscan扩大了受众(横向),但仍然面临严峻的纵向问题:目前的医学体系,还不知道如何科学地解读“变化”。
已有部分研究小组开始评估动态监测对患者预后的影响。
这篇文章:振动控制瞬态弹性成像评分用于预测脂肪性肝病中肝脏相关事件,作者是VCTE-Prognosis Study Group (全球最大的FibroScan队列研究组) 得出以下核心结论 (此处让ai给你们简化了,保证谁都能看懂,有兴趣的读者请看原文):
1.测得准: 基于FibroScan数据的“Agile评分”非常好用,能精准预测脂肪肝患者未来会不会出大事(比如肝硬化、腹水等)。
2.稳得住: 这个评分很稳定,短期内反复测,结果不会忽上忽下。
3.“双重确认”更保险: 与其信一次,不如信两次。如果患者连续两次测量分数都低,那就说明他是真的安全。所以在医生决定要不要给患者做痛苦的“肝穿刺”或者上猛药之前,强烈建议先用FibroScan复测一次。
4.能替代金标准: 这项研究证明,以后在医院看病,甚至在药厂做新药研发(2b/3期临床试验)时,完全可以用无创的FibroScan来代替有创的肝穿刺(活检)。
也有研究评估了FibroScan对于用药连续监测的价值,这个下回讲把。
为什么我这么关心动态监测的价值?一是动态监测直接与患者做Fibroscan的次数挂钩,患者每多做一次Fibroscan就多一份收入;二是动态监测是爱科森区别于海斯凯尔以及其他厂商的重要手段。如果还是停留在“诊断”层面,有没有脂肪肝做个B超就能看,查纤维化海斯凯尔也能凑活用;未来一定是将Fibroscan纳入代谢病全病程管理中,二是配合GLP-1药物做用药动态监测,真正发挥爱科森数据的价值。就算以后进来吴斯凯尔还是其李斯凯尔,他们最多只能干“诊断”这种一锤子买卖,全病程管理这种有壁垒的检测其他企业根本进不来,就算VCTE专利失效他们也没办法
爱科森肝脏数据杂谈之二——动态监测的价值
2025年8月FDA接受LSM by VCTE作为MASH临床试验的首个替代终点意向书,标志着无创监测范式的转折。但LSM作为替代终点的资格认定,本质上是在”完美”与”可行”之间的妥协——它解决了重复肝活检的伦理困境和患者依从性问题,但同时也引入了新的不确定性。
什么不确定性呢?最近的MAESTRO-NAFLD-1试验2年随访数据显示,resmetirom治疗组LSM显著下降,这种改善早于组织学纤维化改善出现。那么就存在一个问题:LSM下降是否真正反映了胶原沉积的减少,还是部分归因于肝细胞脂肪变性、炎症活动度的改善?从病理生理学角度,肝脏硬度受多种因素影响,包括细胞外基质积累、肝窦充血、炎症浸润、胆汁淤积等。将LSM简单等同于纤维化程度,可能过于简化了肝脏病变的复杂性。
简单来说,患者在使用药物后,肝脏脂肪含量迅速下降,炎症标志物(如ALT/AST)改善,这种去脂和抗炎作用迅速降低了肝脏的“张力”和“水肿”,导致LSM读数在短时间内显著下降。此时,肝脏内的胶原纤维网络(真正的纤维化支架)可能尚未发生物理性降解(这通常需要数年)。
因此这就引出了第一个问题:如果将LSM下降作为替代终点,我们可能是在奖励那些擅长消炎去脂的药物,而误以为它们“逆转了纤维化”。虽然消炎去脂本身对预后有益,但如果药物不能阻止胶原沉积的长期进程,LSM的早期改善就是一个“海市蜃楼”。
但随着Resmetirom等药物上市与GLP-1药物MASH适应症获批,要求患者在安慰剂对照试验中进行多次侵入性肝活检变得越来越不符合伦理,且患者招募极度困难。且肝活检本身也有显著的采样误差和观察者间差异。有时候,LSM的动态变化甚至比“金标准”活检更能反映全肝的病理生理状态。
那么如何应对这种不确定性?
一是不单独依赖LSM。LSM与其他血液生物标志物等组成复合评分,以区分“硬度下降”是主要源于脂肪/炎症消退,还是真正的纤维化逆转。
二是重新定义阈值。针对强效去脂药物,可能需要制定更严格的LSM下降阈值(例如下降30%以上),才能被视为纤维化改善的替代指标,而不仅仅是统计学差异。
从科学严谨性角度,替代终点的黄金标准是”充分验证”,即证明替代终点的变化能够完全预测临床终点的变化。但在MASH领域,这种”充分验证”面临时间和伦理的双重困境——肝硬化失代偿、肝移植、肝癌等硬终点需要5-10年甚至更长时间才能观察到,而要求患者在如此长周期内接受安慰剂对照已经越来越不可行。
因此,FDA接受了爱科森的意向书(LOI),采用了”reasonably likely surrogate endpoint”这一相对宽松的标准——只需证明替代终点”合理可能”预测临床获益,而非”确证”预测。这一妥协的代价是不确定性的增加。Resmetirom的MAESTRO试验数据显示,治疗组LSM在52周时显著下降,这种改善早于组织学纤维化改善出现。从监管角度,这足以支持加速批准;但从科学角度,需要证明LSM的早期下降确实转化为长期的临床获益(即减少肝硬化失代偿、肝移植和死亡)。
这种不确定性并非LSM特有的问题,而是所有替代终点共同面临的挑战(因此替代终点审批时间最长,牵扯东西多)。心血管领域的LDL-C降低、糖尿病领域的HbA1c改善,都经历了从”替代终点”到”验证终点”的漫长过程。关键在于建立持续的验证机制:通过真实世界数据、上市后研究、长期队列随访,不断检验LSM变化与临床结局的关联性。
动态监测的核心价值
第二个问题是测量变异性。VCTE LSM的相对重复性系数较高(相比于MRI),这意味着在两次间隔14天的检查中,即使疾病状态完全相同,LSM也可能因测量误差波动超2KPa。对比已确立的治疗应答阈值,这在实践中制造了巨大的灰区。
需要注意的是,几乎所有医疗仪器都有测量误差,测量变异性问题的本质在于单次测量的不确定性——即使疾病状态完全相同,LSM也可能因测量误差波动超2 kPa。但这并不意味着VCTE动态监测失去价值,恰恰相反,这凸显了纵向监测的不可替代性。单次测量是一个数据点,而纵向监测构建的是一条轨迹曲线。轨迹分析的统计学逻辑在于:随机误差是无方向性的,会在时间序列中相互抵消;而真实的疾病进展或治疗应答则必然表现为持续的趋势。这就是为什么FDA最终接受LSM作为替代终点——尽管单次测量存在噪音,但纵向变化的方向性仍然具有预后预测价值。
这种价值在多个队列研究中得到验证。全球超过16,000例患者的数据显示,LSM增加≥30%与肝脏不良结局风险显著升高相关,而LSM下降≥20%的患者肝脏相关事件风险降低至HR 0.42。关键在于,这些阈值的确立本身就考虑了测量变异性——30%的变化阈值远超单次测量的变异范围,确保了信号强度超过噪音水平。更深层的理解是:LSM的绝对值可能受多种因素干扰,但LSM的变化趋势相对稳健,因为那些瞬时性混杂因素(餐后状态、轻度炎症波动)在多次测量中趋于平均化,而真实的病理改变(胶原沉积或降解)则持续累积并最终主导信号。
从病理生理学角度理解,动态监测揭示的是疾病的”速度”而非”位置”。一个LSM为10 kPa的患者,如果6个月后变为12 kPa,12个月后变为14 kPa,这条上升轨迹传递的信息远超任何一个单点数值——它提示代谢失控、炎症-纤维化级联激活、疾病处于活跃进展期。即使考虑到±2 kPa的测量误差,连续三次测量均上升的概率仅12.5%(若完全随机),这种趋势的统计显著性不容忽视。相反,一个基线LSM为15 kPa的患者,如果在治疗后持续稳定在14-16 kPa范围内波动,这种”平稳轨迹”本身就是有价值的信息——提示疾病虽未逆转,但至少得到控制,避免了失代偿的快速进展。
MASH患者的疾病轨迹存在显著异质性,这种异质性远超传统的病理分期所能捕捉。两个基线均为F2期、LSM均为10 kPa的患者,一年后的结局可能截然不同:一个进展至F3期、LSM升至15 kPa,另一个改善至F1期、LSM降至7 kPa。这种差异的驱动因素包括代谢控制、遗传易感性、肠道微生态、环境暴露等多维因素,单次基线评估无法预测。动态监测的价值在于,它能够在疾病自然史的早期阶段识别”高危进展者”,而不是等到失代偿症状出现时才介入。
轨迹表型的概念在多发性硬化症、阿尔茨海默病等神经退行性疾病领域已被广泛应用。通过生长混合模型(Growth Mixture Model)对纵向数据建模,可以识别患者所属的典型轨迹类型——快速进展、缓慢进展、稳定、改善。MASH领域同样适用这一范式。假设存在三种典型轨迹:(1)”快速进展者”——基线LSM中等但斜率陡峭,12个月内上升>5 kPa;(2)”稳定者”——LSM在±2 kPa范围内波动,无明确趋势;(3)”应答者”——治疗后LSM持续下降≥30%。这种分类的临床意义在于,它将患者从”同质化”的纤维化分期中解放出来,转而基于疾病的”动态演进模式”进行分层。
快速进展者即使当前纤维化程度尚轻(F1-F2),其未来进展至肝硬化的风险可能远超稳定的F3期患者。这种”速度风险”在传统静态分期中被完全忽略。原发性胆汁性胆管炎(PBC)领域的研究已经证实,纵向LSM变化可独立预测严重不良事件风险,甚至优于基线LSM值。这提示我们,动态监测捕捉的不仅是”当前状态”,更是”演进轨迹”——而后者在预后预测中可能具有更高的权重。
从更深层次理解,动态监测代表了医学从”疾病分类学”向”疾病过程学”的认识论转变。传统医学强调诊断——将患者的症状和检查结果归类到某个疾病类别(如”MASH F2期”),这种分类学思维适用于急性疾病或稳定状态。但对于进展性慢性病,疾病不是一个静态的”标签”,而是一个动态的”过程”。MASH从单纯性脂肪肝进展至MASH、进展期纤维化、肝硬化、失代偿,是一个连续的演进轨迹,每个患者在这条轨迹上的位置、速度、方向都不同。
动态监测的本质是将疾病从”名词”转化为”动词”——不再问”这个患者是F几期”,而是问”这个患者的纤维化是在进展、稳定还是逆转”,将医疗干预的目标从”改变诊断标签”(如从F2降至F1)转向”改变疾病轨迹”(如从快速进展转为稳定或改善)。后者更贴近患者的真实预后需求——患者关心的不是病理报告上的纤维化分期,而是未来10年、20年是否会进展至肝硬化失代偿。动态监测提供的正是这种”未来导向”的信息。
单次测量的精确度重要,但更重要的是趋势的方向性。即使每次LSM测量存在±2 kPa的误差,只要测量次数足够多、时间跨度足够长,真实的疾病轨迹仍会从噪音中浮现。这类似于气候学研究——虽然每日气温波动剧烈且难以预测,但通过数十年的纵向数据,全球变暖的趋势仍然清晰可辨。MASH动态监测遵循同样的逻辑:单点波动不重要,重要的是跨越时间的累积信号
爱科森肝脏数据杂谈之三——常见慢病管理方式
1. 糖尿病监测:DCCT 定义的两个世界
1993年,《新英格兰医学杂志》发表 DCCT(糖尿病控制与并发症试验)结果的那一天,内分泌医生意识到过去十年的临床实践可能都错了。
在 DCCT 之前,糖尿病管理关注的是什么?大多数患者每天只做一次尿糖测试——不是血糖测试。一项 1989 年的调查显示,只有 45% 的 1 型糖尿病患者每天至少测量一次血糖,57% 的患者从未听说过 HbA1c(糖化血红蛋白)。医生每 3 个月见患者一次,询问症状、调整胰岛素,但缺乏衡量长期血糖控制的客观指标。
HbA1c 虽然在 1977 年就开始用于临床评价,但不同实验室的结果曾因检测方法不同(离子色谱法、亲和层析法等)而出现 2-3 个百分点的偏差,无法横向比较。直到 DCCT 证明了 HbA1c 与并发症风险的直接线性关联,标准化才变得紧迫。1996年,国家糖化血红蛋白标准化计划(NGSP)正式实施,其核心目标就是让全球实验室的 HbA1c 结果能统一对应于 DCCT 的参考值。
DCCT 改变的不仅仅是检测标准,更是监测的哲学。在试验中,强化治疗组设定了近乎严苛的目标——将 HbA1c 控制在非糖尿病人群范围(<6.05%)。尽管在实际操作中,受限于低血糖风险,强化组最终达到的 HbA1c 中位数约为 7.2%(对照组为 9.1%),但这已经足以产生惊人的获益:视网膜病变风险降低了 76%,神经病变风险降低了 60%,微量白蛋白尿发生率降低了 39%。
试验结果公布后,相关指南迅速调整。美国糖尿病协会(ADA)指南迅速调整:从“避免急性症状”转向“预防长期并发症”。监测指标从单纯的“空腹血糖”升级为“每日多次血糖 + 每 3 个月 HbA1c”。
然而,随着HbA1c金标准地位的确立,临床医生逐渐发现了一个令人困惑的现象:为什么同样是HbA1c控制在7%的两位患者,结局却截然不同?一位患者病情稳定,而另一位却频发严重低血糖,甚至早早出现了心血管并发症。
这暴露了HbA1c作为“平均值”的先天缺陷——它掩盖了“波动”。就像一个人的头在火炉里,脚在冰窖里,他的“平均体温”可能是正常的,但人已经不行了。医学界开始意识到,HbA1c完全相同的患者,其血糖形态可能存在天壤之别:是全天平稳,还是在“严重低血糖”与“极度高血糖”之间剧烈震荡?
2000年代的研究开始关注’血糖波动性’(Glycemic Variability)的潜在危害。体外和动物研究显示,间歇性高血糖相比持续高血糖可能激发更强的氧化应激反应,导致更严重的血管内皮损伤。然而,在临床实践中,血糖波动作为糖尿病并发症独立危险因素的证据仍存在争议。尽管如此,这些研究促使医学界开始重新思考:仅关注HbA1c这个’平均值’是否足够?
正是为了解决这个“平均值的谎言”,监测技术必须完成从“照相机”到“摄像机”的进化。
2019 年,国际共识推荐使用“目标范围内时间”(TIR)作为新指标(定义为血糖在 70-180 mg/dL 范围内的时长占比,大多数成人目标为 >70%,及每天至少监测约17小时)。这一转变的驱动力是 CGM(连续血糖监测)技术,它揭示了 HbA1c 无法反映的“血糖波动性”。如今,医生不再满足于“平均值”达标,而是追求血糖曲线的“平稳”。
我国糖尿病患者数量约为2.33亿,这意味着将近1/7的人有糖尿病,也意味着大部分人至少认识一个糖尿病患者,看到这里的读者可以去问问身边“糖友”,看看糖尿病的慢病管理是怎么做的。
2. 肺结节监测:如何找到真正的恶性肿瘤?
肺结节管理的根本困境在于:单次 CT 扫描本质上只是一个“时间切片”。它能精确描述此时此刻病灶的形态、密度和大小,却无法回答最关键的问题:这个结节未来会怎样? 在某个静止的瞬间,良性疤痕和早期恶性肿瘤可能呈现出几乎相同的影像特征。就像仅凭一张照片无法判断一个人的性格,单次测量也无法为肺结节定性。因此,引入时间维度,不是为了最终给出一个确诊结论,而是建立一套理性的“风险管理体系”——让那些不需要干预的病灶通过稳定性自证安全,让真正危险的病灶在动态观察中逐渐暴露本质。Fleischner 指南的演变史,本质上就是医学界逐渐承认单点局限,并学会利用时间来筛选风险的过程。
2005 年,Fleischner 学会发布第一版指南时,CT 技术刚刚进入薄层时代。面对突然涌现的海量微小结节和静态不确定性,指南被迫采取了“宁可错杀,不可漏网”的保守策略:对 4mm 甚至更小的结节也建议随访。因为在当时缺乏动态数据,无法区分哪些是静止的淋巴结,哪些是早期的癌症。
然而,随后的十几年里,临床数据揭示了这种“过度监测”的代价——大量患者承受了无意义的辐射和焦虑。2013 年,针对磨玻璃结节(GGN)的指南率先做出调整。尽管早期研究(如 Henschke 等)显示部分实性结节的恶性概率可达 63%,但这类病灶生长极慢,倍增时间(VDT)往往长达数年。指南据此提出了“监测节奏应与肿瘤生物学行为匹配”的理念:对于这种“慢性子”的病灶,即使是恶性的,也可以从容观察,而非机械地进行高频复查。
2017 年,Fleischner 指南迎来了最关键的转折:将需要常规随访的最小结节尺寸从 4mm 提高到 6mm。这一调整基于 NLST(美国国家肺筛查试验)和 NELSON 等大规模筛查研究的证据:在高危人群中,<6mm 结节的恶性风险实际上低于 1%。对于这类低风险结节,过度频繁的 CT 检查带来的辐射风险和心理焦虑,远超其潜在获益。
以磨玻璃结节(GGN)为例,尽管早期研究显示部分实性病灶的恶性概率可高达 60% 以上,但后续的大规模追踪发现,这类病灶即使确为恶性,其倍增时间(VDT)也往往长达数年。这意味着“恶性概率高”并不等同于“需要紧急处理”。监测的节奏应当与肿瘤的生长速度相匹配,而非机械地仅凭尺寸或影像特征进行“一刀切”。
更具颠覆性的发现是,某些特定形态的结节——例如那些位于叶间裂附近、边界光滑的实性小结节——经过多年追踪证实几乎没有恶变风险,它们实际上只是肺内淋巴结的正常表现。这些循证医学证据推动了监测策略的调整:将需要常规随访的最小尺寸阈值上调,并对具有典型良性征象的结节明确豁免随访,真正实现了基于风险分层的差异化管理。
这一转变的核心逻辑,是用大规模真实世界数据来量化“单次测量无法定性”这一根本矛盾下的边界。医学界逐渐认识到,动态监测的价值不在于追求 100% 的即时确定性,而在于识别出那些真正需要“时间”来显露本质的病灶。对于极低风险的微小结节,稳定观察本身就是最好的处理;对于中等风险的病灶,合理的监测间隔既能捕捉到有意义的变化,又能避免过度干预;只有那些在观察中表现出生长趋势或高危特征的结节,才需要进一步的诊断性操作。
肺结节的动态监测,本质上是承认单次测量的局限性,用时间来弥补空间信息的不足,最终目的是在风险控制与过度医疗之间找到最优的平衡点。
因此,对于有肺结节的读者来说,找一个靠谱的胸外科医生与符合指南要求的随访频率至关重要(很不幸本人也有)。
3. 慢性肾病监测:从静态分期到动态轨迹
慢性肾病(CKD)的分期系统最初建立在2002年美国国家肾脏基金会肾脏病预后质量倡议(NKF-KDOQI)指南上。这一系统主要依赖估算肾小球滤过率(eGFR)的横断面数值,将CKD分为5个阶段(G1至G5),其核心假设是:eGFR低于60 mL/min/1.73m²持续3个月或以上,无论是否存在肾脏损伤标志物,均应诊断为CKD。当时的逻辑基础是,相同分期的患者面临相似的风险,因此应采取一致的监测频率和治疗策略。
然而,临床实践很快揭示了这一简化模型的局限性。2012年KDIGO指南引入了重大改革,推荐基于病因(C)、GFR分类(G)和白蛋白尿分类(A)的”CGA”三维分类系统。GFR第3类被进一步细分为3a(45-59 mL/min/1.73m²)和3b(30-44 mL/min/1.73m²),因为大量数据表明这两个亚组在预后和风险方面存在显著差异。白蛋白尿被划分为三个等级:A1(<30 mg/g)、A2(30-300 mg/g)和A3(>300 mg/g) ,形成了一个综合的风险评估矩阵。
针对大型队列的深入研究打破了CKD进展必然呈线性下降的传统观念。在非洲裔美国人肾脏病与高血压研究(AASK)中,对846名患者长达12年的随访显示,352名患者(41.6%)具有大于0.9的概率表现为非线性轨迹或长期非进展期;在559名患者(66.1%)中,这一概率超过0.5。这些发现表明,仅凭静态eGFR值,两个数值相同的患者可能面临截然不同的疾病轨迹:一个可能多年稳定,另一个可能正经历肾功能的快速恶化。
在今天的肾脏病学实践中,eGFR 斜率(eGFR Slope)正成为核心关注点。医生不再只问他现在肾功能剩多少,而是问他每年丢失多少。对于 eGFR 年下降率超过 5 mL/min/1.73m² 的患者,即使当前分期尚早,也被视为极高危人群,需要加密监测并启动强化干预。这种从“静态位置”到“动态速度”的视角转换,是精准医学在慢病管理中的典型体现。
4. 颈动脉斑块监测:从恐慌筛查到循证决策
2000 年代初期,随着超声技术的普及和便携设备的出现,颈动脉斑块筛查曾经历过一段“狂野生长”的时期。商业化的移动筛查车开进社区,不分年龄、症状或危险因素,对大量无症状人群进行扫描。这种“广撒网”的结果是,无数健康人被贴上了“动脉硬化”的标签,陷入长期的健康焦虑。更严重的是,假阳性或非必须的阳性结果触发了后续侵入性检查(如血管造影)甚至预防性手术,带来了出血、卒中甚至死亡的医源性风险。过度筛查被精准地定义为:“在无症状人群中进行检查,但检查结果不会改善其健康状况。”
理性的回归始于权威机构的“踩刹车”。
美国预防服务工作组(USPSTF)在 2014 年及 2021 年的更新中,连续给予无症状颈动脉狭窄筛查 D 级推荐(反对筛查)。其核心逻辑在于:虽然颈动脉狭窄是卒中的危险因素,但在无症状人群中其患病率仅约 1%,且仅导致了约 10% 的缺血性卒中。对于大多数人而言,盲目筛查带来的过度干预远超其潜在获益。
与此同时,临床关注的焦点从单纯的狭窄程度转向了斑块性质。传统的血管水管工思维认为,管腔堵得越死,风险越大。但最新证据表明,大多数神经系统症状实际上出现在狭窄程度 <70% 的患者中。这催生了易损斑块(Vulnerable Plaque)理论:决定卒中风险的往往不是斑块的大小,而是它的稳定性(如是否有脂质坏死核心、斑块内出血或表面溃疡)。
这一理论深刻改变了监测的逻辑。对于已经接受他汀等规范治疗的患者,反复用超声测量斑块的大小往往是徒劳的。一项纳入 566 名患者的荟萃分析显示,他汀治疗后的主要变化是斑块回声增强(意味着钙化、变硬、稳定),这种“质”的改变往往早于“量”(体积缩小)的改变。这意味着,如果治疗目的是“稳定斑块”,那么盯着狭窄率的微小波动就没有临床意义。
现在的临床策略已经转变为以决策为导向的监测:对于低危/稳定群(已规范治疗、依从性好),不再建议频繁复查,因为结果不会改变目前的药物治疗方案。对于高危/易损群(斑块形态不稳定、溃疡、或狭窄率处于手术临界值),则保持密切的动态监测,以捕捉手术干预的窗口期。
这一转变再次印证了一个朴素的真理:监测本身不是治疗。只有当监测结果能指导医生调整治疗方案时,监测才具有医学价值。盲目的筛查和无意义的复查,不仅浪费医疗资源,更是对患者心理防线的无谓消耗
本来近期打算就是躺平,计划等公司交流会之后再写文章,结果你倒好,真奔着缺口去了,是美法关系破裂了还是工厂搬到德黑兰了,还是管理层滞留中东回不来了?昨天晚上我还在吃瓜伊朗导弹到底炸没炸中美国航母,现在搞清楚了,是精准炸中我账户了![]() 。一个春节不见你变成美伊概念股,逻辑是不是战争导致伊朗人挨饿,脂肪肝消失了,不用做Fibroscan检查了。哎!
。一个春节不见你变成美伊概念股,逻辑是不是战争导致伊朗人挨饿,脂肪肝消失了,不用做Fibroscan检查了。哎!
好了,言归正传,本来应该接着上回写指南相关问题的,鉴于一大堆人问我GE的新设备到底咋回事,那我谈谈看法吧。至于公司港股上市是不是出问题,我只能说,我也很想知道,建议认识老王的打电话问问。
1.如何评估MASLD病情
在过去,NAFLD被简单地分为两大类:单纯性脂肪肝和非酒精性脂肪性肝炎(NASH)。前者被认为是”良性”的,预后较好;后者则可能进展为肝硬化和肝癌。这种分类方式看起来很清晰,就像把患者分成”好”和”坏”两类。但在临床实践中,这种简单的二分法存在诸多问题。
首先,疾病进展本质上是一个动态连续的病理过程,炎症活动度与纤维化程度的演变并非存在截然分明的阶段性跳跃,人为的二元划分无法准确反映疾病的自然史。其次,不同患者在脂肪变性程度、炎症活动度及纤维化程度之间的组合特征存在显著异质性,单一维度的分类难以涵盖复杂的临床表型。更为关键的是,长期随访数据表明,相当比例被诊断为”单纯性脂肪肝”的患者最终仍进展为肝硬化,”单纯性”这一术语在客观上赋予了患者及临床医生虚假的安全感,可能导致随访管理的松懈。
基于上述认识,2023年多学会专家共识及EASL-EASD-EASO 2024年指南建议摒弃简单的二分类法,转而从肝脏脂肪变性程度、肝脏炎症活动度、肝纤维化程度三个相互独立又彼此关联的维度对疾病严重程度进行连续性、量化评估,以实现更为精准的风险分层与个体化管理。
2.MASLD指标之一:肝脏脂肪变性程度(脂肪肝)
肝脏脂肪变性程度的评估,是MASLD诊断与分级体系的起点与基础。所谓”脂肪变性”,是指肝细胞内脂质(主要为甘油三酯)异常蓄积,超过正常生理范围的病理状态,也就是大家常说的“脂肪肝”。
病理学分级:金标准,难以在实践中推广
在所有评估手段中,肝活检病理学检查至今仍是脂肪变性分级的金标准。目前国际上普遍采用NASH CRN评分系统,以发生脂肪变性的肝细胞占全部肝细胞的比例作为分级依据,将脂肪变性分为四个等级:
分级含义 S0无脂肪变性 脂肪变性肝细胞比例<5%S1 轻度5%~33% S2中度34%~66% S3重度>66%
然而,肝活检毕竟是有创操作——穿刺出血、疼痛、极少数情况下的严重并发症,加之采样误差(一根穿刺针仅能取到全肝约1/50000的组织),使其难以在常规临床实践中大规模推广,更不适合用于疗效的动态随访监测。
无创影像学评估:各有所长,按需选用
① 常规腹部超声:普及最广的初筛工具(各指南推荐作为筛查的首选影像学方法)
腹部超声是目前应用最广泛的MASLD初筛手段,EASL-EASD-EASO 2024年联合指南明确推荐其作为疑似MASLD患者的首选影像学筛查方法。其优势显而易见:操作简便、费用低廉、无辐射、可实时动态观察,基层医院即可开展。脂肪肝在超声下表现为肝脏回声弥漫性增强(俗称”明亮肝”),与肾脏皮质回声相比呈高回声改变。然而,常规超声存在明显短板:对轻度脂肪变性(S1级,即5%~33%的肝细胞受累)的检出敏感性较低,主要适用于中重度脂肪变性的识别;更重要的是,它只能定性判断”有没有”脂肪肝,
② FibroScan受控衰减参数(CAP):一站式检测的便捷选择
CAP技术集成于振动控制瞬时弹性成像(VCTE)设备(即FibroScan),可在完成肝脏硬度测量的同时,同步获取肝脏脂肪定量数据,实现”一次检查,两项指标”的高效评估。CAP的工作原理是测量超声波在脂肪组织中的衰减程度,脂肪含量越高,超声衰减越明显,CAP值越大,单位为dB/m。根据大样本荟萃分析,诊断不同程度脂肪变性的推荐界值为:≥S1对应≥248 dB/m、≥S2对应≥268 dB/m、≥S3对应≥280 dB/m,整体诊断准确性(AUC)在0.82~0.89之间。需要注意的是,CAP测量结果以dB/m为单位,与病理学的细胞比例(%)和MRI的脂肪体积分数(%)在量纲上并不一致,跨方法横向比较时需谨慎解读;此外,肥胖患者(BMI过高)可能影响探头穿透深度,导致测量失败或结果偏差。
③ 超声衍生脂肪分数(UDFF):新一代定量超声的后起之秀
UDFF是近年来兴起的新一代定量超声技术,集成于常规超声诊断系统,无需专用设备,操作流程与普通超声基本相同。其最大亮点在于:测量结果直接以百分比(%)表示,与MRI-PDFF的单位完全一致,临床医师和患者均可直观理解,也便于不同时间点的纵向随访比较。2025年发表的一项来自中国、迄今规模最大的前瞻性多中心研究纳入790例疑似MASLD患者,系统验证了UDFF的诊断价值,推荐界值为:≥S1对应≥8%、≥S2对应≥14%、S3对应≥20%,各级别诊断的AUC达0.85~0.95,重复性良好,在不同中心、不同操作者之间均表现出较高的一致性。这一特性使UDFF在基层医院推广和大规模人群筛查方面具有显著优势。
④ MRI质子密度脂肪分数(MRI-PDFF):无创评估的替代金标准
MRI-PDFF是目前公认的无创评估肝脏脂肪含量的替代金标准,其诊断准确性在所有无创方法中最高。该技术通过多回波化学位移编码MRI序列,精确测量肝脏内质子信号中来自脂肪的比例,以≥5%作为诊断脂肪变性的界值(与病理学S1级的起始阈值相对应)。MRI-PDFF能够覆盖全肝多个感兴趣区,有效克服肝活检的采样误差问题;同时,其测量结果受肥胖、腹水等混杂因素的影响相对较小,在不同厂家设备之间的一致性也较好。然而,MRI检查费用昂贵、检查时间较长、设备可及性有限(尤其在基层医疗机构),使其在常规临床筛查中的应用受到制约。
3.MASLD指标之二:肝脏炎症活动度
如果说脂肪变性是MASLD的”入场券”,那么炎症活动度则是决定疾病走向的”分水岭”。当肝细胞内脂质蓄积超过一定阈值,多余的脂质代谢产物(如游离脂肪酸、神经酰胺等)会对肝细胞产生直接毒性,触发氧化应激与线粒体功能障碍,进而激活天然免疫系统,引发持续性肝脏炎症反应。一旦炎症持续存在,活化的Kupffer细胞(肝脏驻留巨噬细胞)和浸润的单核细胞会释放大量促纤维化细胞因子(如TGF-β、PDGF),激活静息状态下的肝星状细胞,使其转化为活跃的成纤维细胞,持续分泌胶原蛋白,最终驱动纤维化乃至肝硬化进程。
病理学评估:MASH诊断的金标准
肝活检是目前确诊MASH的唯一金标准。病理医师需在显微镜下同时确认三项特征:脂肪变性、小叶内炎症浸润、肝细胞气球样变(细胞肿胀变形,是肝细胞受损的直接形态学标志),三者缺一不可。临床研究中常用**NAFLD活动性积分(NAS)**进行量化,总分0~8分,NAS≥5分与MASH诊断高度相关;但NAS本质上是活动度量化工具,不能单凭总分替代对三项组织学特征的综合判断。
在大多数常规临床情境下,肝活检并非必要。无创评估策略在临床实践中占据着更为核心的地位。
无创评估:主要是血清生物标志物
由于肝活检有创、存在采样误差且不适合动态随访,无创评估在日常临床中更具实用价值,主要包括以下几类:
血清CK-18片段:肝细胞凋亡或坏死时释放入血,是目前诊断MASH证据最充分的单项生物标志物,诊断AUC约0.78~0.82,但国内检测普及度有限。
ALT/AST:经典的肝细胞损伤标志物,动态监测价值明确,但特异性不足——相当比例的MASH患者转氨酶可在正常范围内。
ELF评分:整合透明质酸、PIIINP、TIMP-1三项基质重塑指标,主要用于纤维化评估,同时对识别具有进展风险的MASH患者及预测长期预后有辅助价值。
弹性成像:活动性炎症可独立于纤维化之外导致肝脏硬度升高,解读时需结合炎症指标综合判断,避免误判为纤维化加重。
无创评估的局限与肝活检的保留价值
需要明确的是,现有无创手段尚不能精确量化炎症活动度,其主要价值在于风险分层与长期预后预测,而非对炎症程度的精确判定。在以下情形下,肝活检仍不可替代:需明确诊断MASH、排除自身免疫性肝病或药物性肝损伤等其他病因,以及在临床试验中评估新型药物的组织学疗效。
4.MASLD指标之三:肝纤维化程度
在MASLD的三大评估维度中,肝纤维化程度是预测长期预后最重要的指标。多项大型前瞻性队列研究已证实,基线纤维化分期是肝脏相关死亡与全因死亡的最强独立预测因子,其预后价值显著优于炎症活动度指标。纤维化的本质是肝星状细胞持续激活后胶原纤维异常沉积的结果;若进程未被有效阻断,最终将演变为肝硬化,显著增加肝功能失代偿与肝细胞癌风险。
这块不用我多写了把,光看前人发的雪球帖子一找一大堆,之前说的无创替代优势,FDA批准的替代终点,跟诺和诺德的战略合作,什么美肝病指南更新等等等等,说的都是检测肝纤维化程度福瑞的设备临床地位有多高。
检测脂肪肝,也就是本贴第一项肝脏脂肪变性程度,所有指南,不管是国内的还是国外的,自始至终推荐的都是超声优先,不然全世界那么多脂肪肝是咋查出来的,现在GE出的设备,能实现超声衍生脂肪分数检测,也就是本贴第一项写的③ 超声衍生脂肪分数(UDFF)。简单来说,原来b超没法定量评估脂肪含量,现在能定量评估了。检测肝纤维化(LSM)和检测脂肪变性(UDFF),是两条完全独立的赛道,用的是不同的物理原理,服务的是不同的临床需求,设备之间没有替代关系。

发表回复